【薬剤師国家試験 第102回 問10】塩基性の強さを比較しよう

塩基性の強さを比較する問題です。
それでは早速、選択肢を1つずつ見ていきましょう。
【1】……カルボキシル基は、もちろん酸性を示す官能基ですよね。
正解候補にはなり得ません。
【2】……この官能基はグアニジノ基と呼ばれており、塩基性を示します。
2番の化合物がプロトン化された場合、次のような共鳴構造式を書くことができます。

つまり、この塩基の共役酸は電子が非局在化しており安定化されているということですよね。
そのため、グアニジノ基は強い塩基性を示すことになります。
【3】……この部分はアミド構造です。
アミド構造は酸性とも塩基性とも言い難く、基本的に中性です。
下に示したように、窒素原子の非共有電子対は、隣接するカルボニル基に引っ張られているためプロトン化を受けづらいのです。

【4】……破線で囲まれた部分は、インドール環です。
インドールは、芳香族性をもつ化合物です。
一見すると、窒素原子の非共有電子対が塩基性を示すように思えますが、どうなのでしょうか?
この点について、考えていきましょう。
下に、インドールの部分の共鳴構造式を示しました。
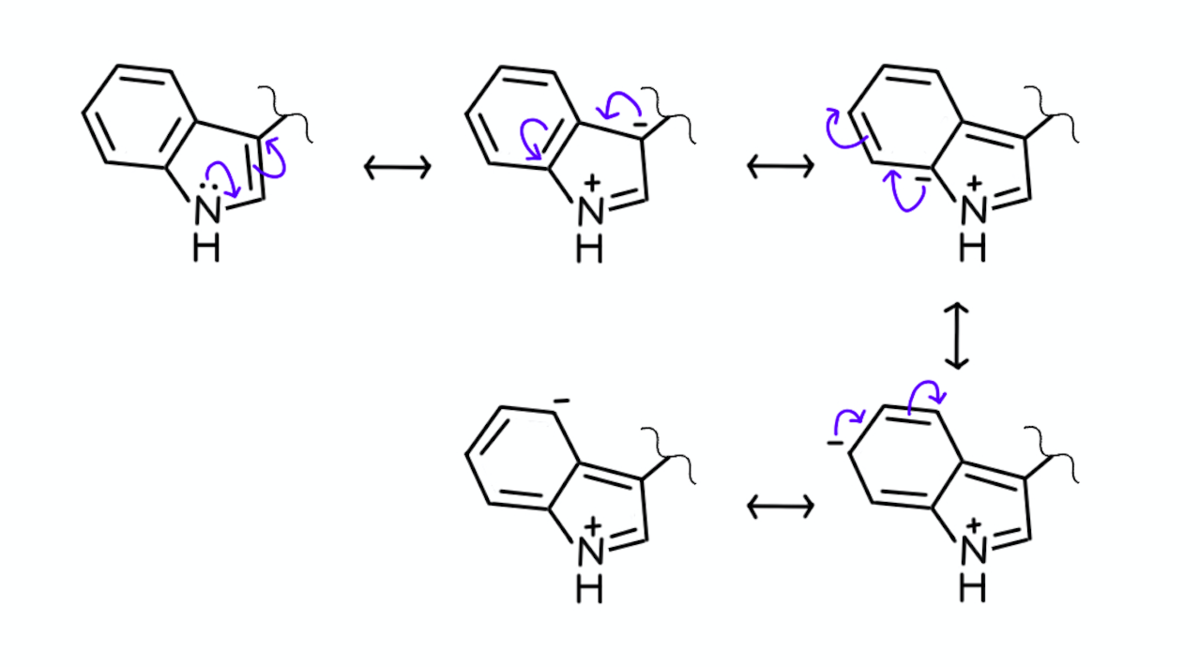
この共鳴構造式から、窒素原子の非共有電子対は環上に非局在化していることが分かります。
ここで、インドール環の上にあるπ電子の数を数えてみましょう。
ベンゼン環のp軌道を占める電子(6π)と、この二重結合のp軌道を占める電子(2π)、そして窒素原子の非共有電子対(2π)を合わせて、10πになります。

「4n+2個のπ電子が環状に非局在化」し、かつ「その環が平面構造である」と、芳香族性を示すんでしたね。*1
芳香族性を示すということは、安定化しているということであり、インドールの部分へのプロトン化は極めて起こりづらいでしょう。
【5】……破線で囲まれた部分は、イミダゾール環です。
この構造の中には、窒素原子が2つあります。
下側の窒素原子の非共有電子対は、【4】のインドールのものと同じように環上に非局在化しています。
一方で、上側の窒素原子の非共有電子対はsp2軌道に入っており、プロトン化されることがあります。

したがって、イミダゾール環は塩基性を示します。
ただし、イミダゾール環よりも、共役酸の共鳴構造式が書くことのできるグアニジノ基の方が塩基性が強いです。
以上のことから、【2】のグアニジノ基の塩基性がもっとも強いです。
正解は、2番の選択肢でした。
なお、第104回の問7にも同じような問題が出題されています。
解説していますので、よかったら参考にしてください(下記リンク)。
chemist-programming.hatenablog.jp
---
興味のある方は是非どうぞ↓
問題の出典: 厚生労働省ホームページ(https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000168886.html)