【大学/薬学部】有機化学ミニ講義 ルイス構造式①
大学の有機化学について基礎的なところから順々に説明していこうと思っています。
まずは、ルイス構造式について説明していきますね。
3つの記事に分けて投稿します。
① ルイス構造式の基本
② 電荷をもつルイス構造式
③ 第105薬剤師国家試験の問6を解きながら補足
それでは早速、ルイス構造式の基本的なところから見ていきましょう。
始めに、とても簡単な分子である H2(水素分子)について解説します。
ルイス構造式を書くために、まずは水素原子Hが結合に使われる電子を何個もっているのかを確認する必要があります。
結合に使われる電子とは……最外殻の電子のことです。
最外殻にある電子を、「価電子」と呼ぶんでしたね。
価電子がいくつあるのか知るためには、原子番号を確認するのがてっとり早いです。
水素の原子番号は1番ですよね。

水素原子を模式的な図で表してみると、下のように陽子を1コ、電子を1コ持っています。

水素原子の場合、この1コが価電子になります。
1s軌道に入っている電子です。
下記のように、2つの水素原子(H)が電子を1つずつ出し合い、水素分子(H2)ができあがります。

今回のテーマである「ルイス(Lewis)構造式」は、このように電子を黒い点で表したものです。
水素分子中の2つの黒い点を1本の線で表すと、下に示したよく見る構造式になります。

こちらの構造式(ちなみに、ケクレ(Kekulé)構造式と呼びます)の方がよく使われると思いますが、有機化合物の構造をしっかりと深く理解するためにはルイス構造式が必要になってきます。
続いて、水分子 H2O のルイス構造式について考えていきましょう。
水素原子については先ほど考えましたので、今度は酸素原子について考えます。
酸素は原子番号が8番です。
ということは、電子を8コ、陽子を8コもっているということですよね(もちろん中性子もあります)。
さて、電子について詳しく見ていきましょう。
1s軌道に2コ、2s軌道に2コ、2p軌道には4コの電子があります。

カッコの中は軌道の名称、上付きの数字はその軌道に入っている電子の数を表しています。
結合の形成に使われる可能性がある電子は、2s軌道の電子2コと2p軌道の電子4コ……つまり、合計6コです。
2コの電子が入っている1s軌道は、貴ガス(希ガス)であるヘリウム He の電子の構造と同様で安定であり、結合には使われません。

酸素原子と結合する水素原子は2コですので、結合に使われる6コの電子のうちの2コの電子が、水素原子との結合形成に使われます。
残りの4コの電子は非共有電子対になる……というわけです。
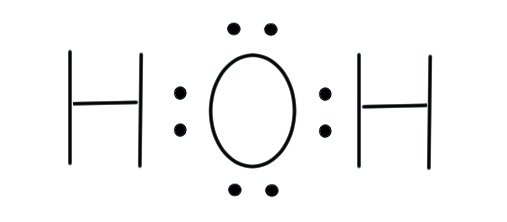
改めて、水分子 H2O のルイス構造式を下に示します。
結合に使われた2コの電子と、使われなかった4コの電子を確認しておきましょう。

最後に、アンモニア(NH3)について考えていきます。

窒素原子が登場しましたね。
窒素の原子番号は7番です。
というわけで、窒素は陽子を7コ、電子も7コもっています。
これら7コの電子は、1s軌道に2コ、2s軌道に2コ、2p軌道に3コ入っています。

先ほどと同様に、1s軌道の2の電子は結合に使われないので、結合に使われる可能性のある電子は5コですよね。
アンモニアの水素原子は3コですので、このうちの3コの電子が結合に使われていて、残りの2コは非共有電子対になるわけです。
改めて、アンモニア分子のルイス構造式を示しておきます。

さて、さらに注目して欲しいことがあります。
それは、NH3の窒素原子の周りには電子が8コある……ということです。
先ほどのH2Oの酸素原子も、やはり周りに8コの電子をもっていました。
両者とも貴ガスで言うところのNeの電子配置[(1s)2 (2s)2 (2p)6]と同様の電子配置になっており安定しているわけです。

これを「オクテット則」と言うんでしたね。
オクテット(octet)は『8個でひとまとまり』という意味です。
「8電子則」と呼ぶこともあります。
オクテット則は、主に第2周期の元素に当てはまりますが、例外もあります。
とくに第3周期になるとd軌道があるので結構複雑になってオクテット則に当てはまるときと当てはまらないときがあるので、ご注意ください。
これで今回の話は終わりです。
次の記事では、電荷をもつルイス構造式について解説していきます。
chemist-programming.hatenablog.jp
---
興味のある方は是非どうぞ↓