【薬剤師国家試験 第103回 問210】配位能を比較しよう
問210はキレートに関する問題です。
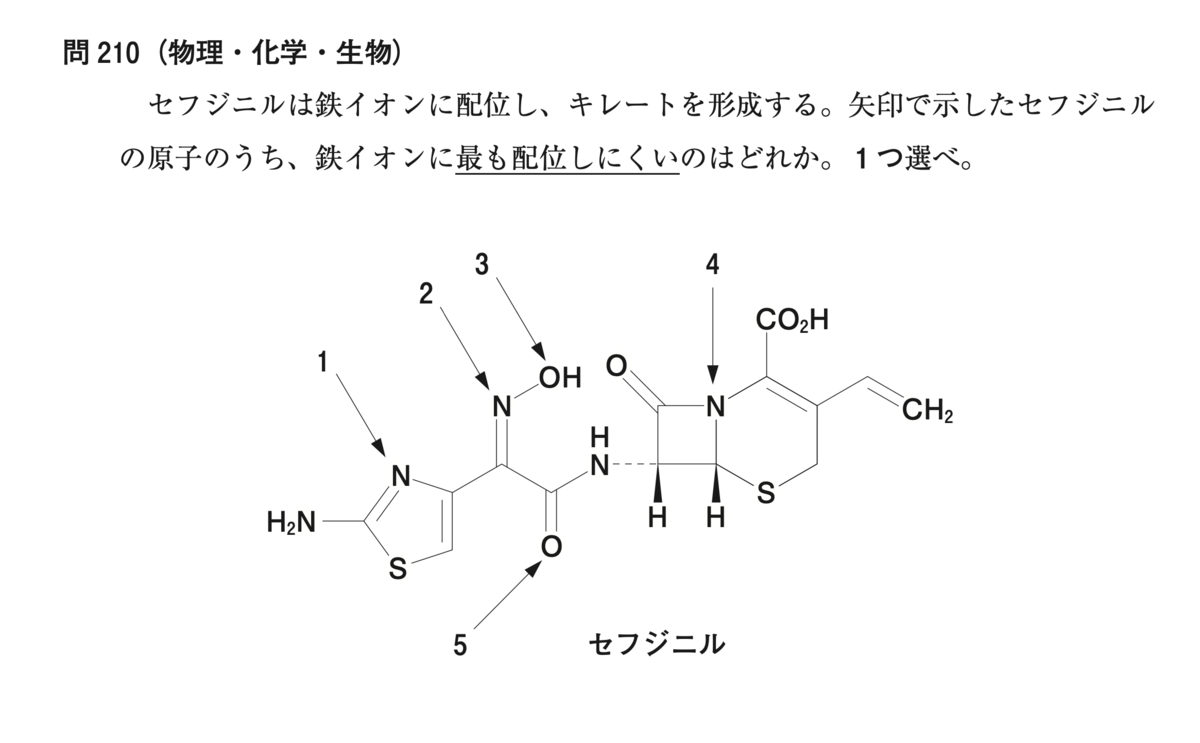
配位子は、基本的に非共有電子対を介して金属イオンに配位しますよね。
このポイントを踏まえて、1〜5の原子がもつ非共有電子対に着目していきましょう。
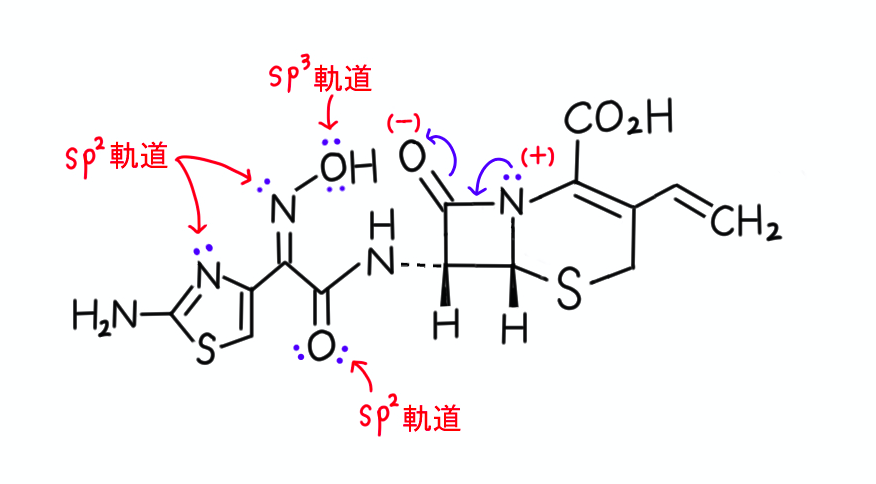
1と2の窒素原子がもつ非共有電子対は、sp2軌道に入っていますよね。
例えば、インドール環の窒素原子の非共有電子対のように、近傍の原子のp軌道を介して非局在化しているわけではありません*1。
ピリジン環の窒素原子がもつ非共有電子対(←塩基性を示す)と同様の状態です。
そのため、1と2の窒素原子の非共有電子対は配位する能力がありそうですよね。
3の酸素原子は、非共有電子対を2組ももっています。
これらの電子は近傍の原子のp軌道を介して非局在化しているとは言い難く、sp3軌道に入っていると考えていいでしょう。
そのため、この酸素原子がもつ非共有電子対は、金属イオンに配位する可能性があります。
4の窒素原子がもつ非共有電子対は、上図に示したように直接結合しているカルボニル基に引っ張られて非局在化しています。
そのため、配位能力は低いと言えます。
5の酸素原子がもつ非共有電子対は、sp2軌道に入っており、非局在化はしていません。
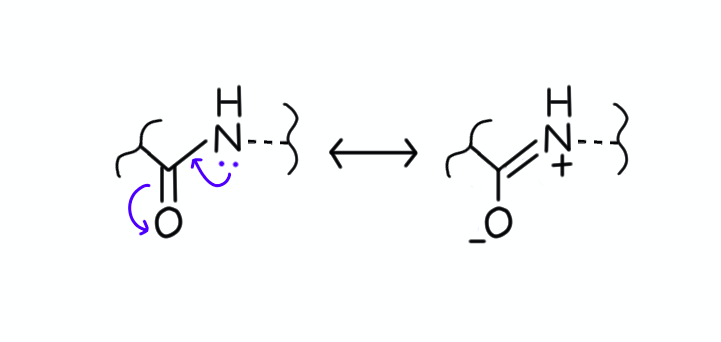
さらに、次のような共鳴構造式が書けます。
5の酸素原子は部分負電荷を帯びているため、配位能力が高いでしょう。
以上のことから、4の窒素原子がもつ非共有電子対が、明らかに配位能力が低いと言えます。
---
YouTubeでショート動画を始めました!
第109回薬剤師国家試験の解説をしていますので、是非どうぞ↓
本ブログの管理人が薬の書籍を執筆しました↓(2024年9月発売)
薬理学を簡単に説明しつつ、有機化学(医薬品化学)も織り交ぜています。
こちらも是非よろしくお願いします!
noteではサイエンスライターとして、薬をはじめとする様々な情報を発信しています↓
こちらもよろしくお願いします。
問題の出典: 厚生労働省ホームページ(https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000198920.html)
*1:参考: リンク先の選択肢5【薬剤師国家試験 第104回 問7】塩基性の強さを比較しよう - ばけがくしゃの勉強ブログ
