【薬剤師国家試験 第103回 問105】酵素と基質の相互作用について考えよう
今回は、酵素の活性部位に関する問題です。
とても難しそうな問題が出題されました。

基質タンパク質のペプチド結合、すなわちアミド結合が、酵素によって加水分解されます。
酵素を構成するアミノ酸のうち、この反応に大きく関わるのが、ヒスチジン(His)、アスパラギン酸(Asp)、セリン(Ser)残基です。
それでは、そのメカニズムを見ていきましょう(下図①〜③)。
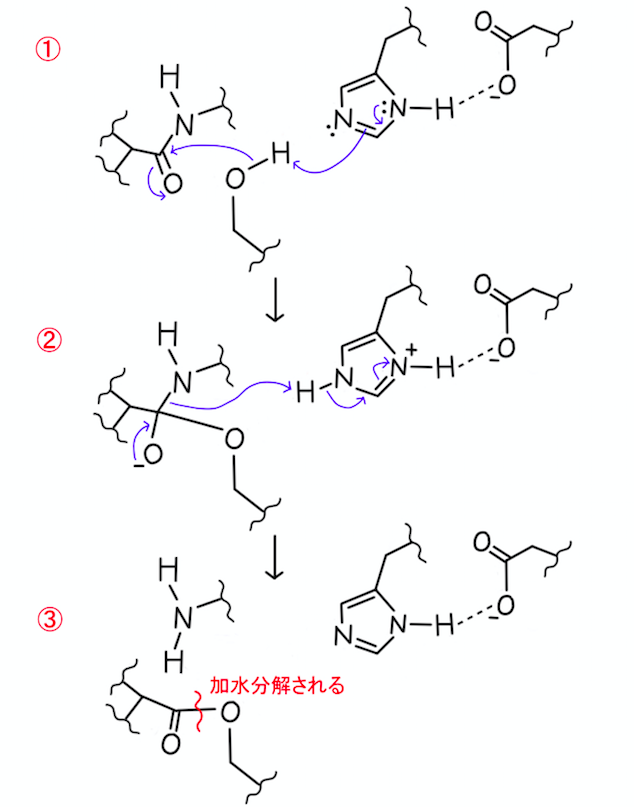
まずは、①の段階です。
巻き矢印を追って見てみると、ヒスチジン残基中のイミダゾリル基は、塩基として働いていることが分かりますね。
この影響によって、セリン残基の水酸基は求核性が高まり、アミド結合のカルボニル炭素に求核攻撃することができます。
続いて、②の段階です。
基質タンパク質と、セリン残基が結合しましたね。
ここで、アスパラギン酸残基の負電荷は、プロトン化されたイミダゾリル基の正電荷を安定化させています。
つまり、イミダゾリル基がセリンからプロトンを奪いやすくしていたのです。
アスパラギン酸残基とイミダゾリル基の間に働く相互作用は、イミダゾリル基の塩基性を高める効果があるわけです。
なお、アミド結合が切断される過程で、ヒスチジン残基に移っていたプロトンは、今度はアミド結合を形成していた窒素原子に移ります。
最後は、③の段階です。
生体内の水分子が求核攻撃し、エステル結合が加水分解されます。
その結果、カルボン酸が生じ、セリン残基は元どおり(R-OH)になります。
このような過程①〜③を経て、基質タンパク質のアミド結合が切断され、カルボン酸とアミンが生じるわけです(生体内では、-COO–と-NH3+ になっていると思われます)。
【1】……①で示したように、イミダゾリル基は塩基として働いて、セリン残基の水酸基の求核性を高めていました。
したがって、この選択肢の記述は正しいです。
【2】……②で示したように、アスパラギン酸残基の負電荷によって、イミダゾリル基の塩基性を高めています。
そのため、この選択肢の記述は間違いです。
【3】基質タンパク質(や低分子)と酵素の相互作用には、いくつかのパターンがあります。
水酸基やアミノ基などの間で生じる「水素結合」や、カルボキシラートイオンとアンモニウムイオンとの間で生じる「イオン結合(塩橋)」などです。
他にも、問題の図に記載されているフェニル基のような疎水性の置換基が、酵素の疎水性ポケットと相互作用することが分かっています。
よって、【3】の記述は正しいです。
【4】セリン残基の役割は【1】で述べたとおりです。
セリン残基の水酸基が、ヒスチジン残基と相互作用しつつ、カルボニル基に求核攻撃するんですよね。
よって、この記述は間違いです。
正解は【1】と【3】でした。
---
YouTubeでショート動画を始めました!
第109回薬剤師国家試験の解説をしていますので、是非どうぞ↓
本ブログの管理人が薬の書籍を執筆しました↓(2024年9月発売)
薬理学を簡単に説明しつつ、有機化学(医薬品化学)も織り交ぜています。
こちらも是非よろしくお願いします!
noteではサイエンスライターとして、薬をはじめとする様々な情報を発信しています↓
こちらもよろしくお願いします。
問題の出典: 厚生労働省ホームページ(https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000198920.html )
