【薬剤師国家試験 第103回 問100】酸素原子の電子数を数えることから始めよう
今回から理論問題に移ります。
問100は非常に難しそうな問題ですが、落ち着いて解いていきましょう。
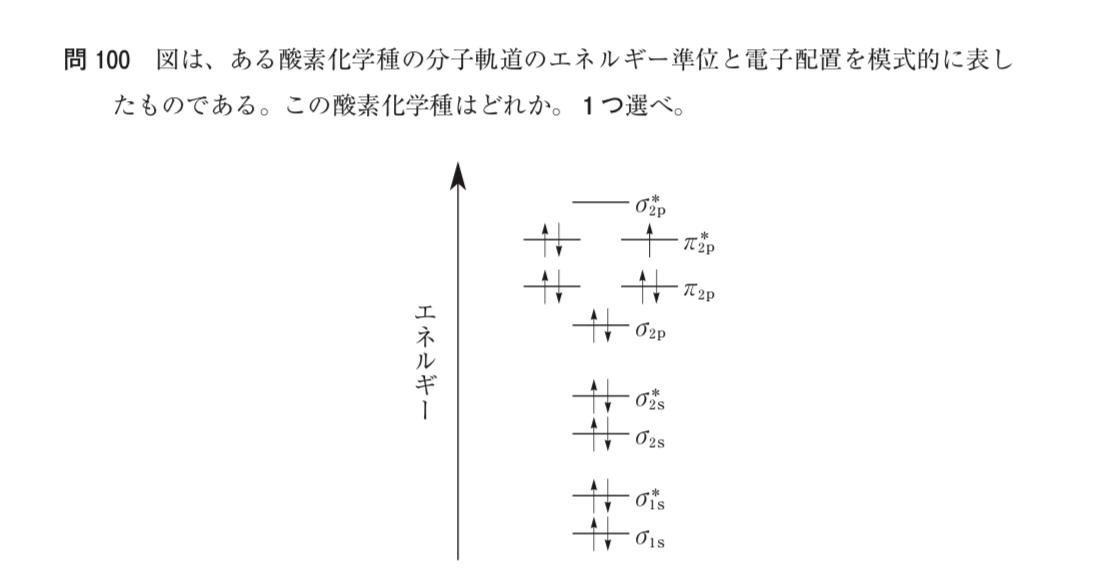

電子(↑と↓)の総数を数えてみると、17個ありますね。
酸素原子(O)の電子数は8なので、酸素分子(O2)ならば電子を計16個もっていることになりますよね。
酸素原子の電子数を覚えていなかったら、H, He, Li, Be, B, C, N, O……と、地道に数えていきましょう。
ということは、酸素原子3つ分(電子24個分)で構成されている5のオゾンは、すぐに除外できます。
また、選択肢1と2の一重項酸素および三重項酸素は、どちらも酸素分子(O2)のことを意味しています。
「一重項」と「三重項」は、電子の状態を表す用語であり、電子の数とは関係がないんでしたね。*1
そのため、一重項酸素と三重項酸素の電子数はどちらも16であり、正解ではありません。
残され選択肢は、3のスーパーオキシドと、4の過酸化物イオンです。
スーパーオキシドの電子数は、イオン式の右上にマイナスが表記されているので、(酸素分子の電子数)+1= 17です。
一方、過酸化物イオンの電子数は、イオン式の右上に2-と表記されているので、(酸素分子の電子数)+2= 18になります。
以上のことから、答えは3番のスーパーオキシドです。
問題の図を見ていると難しそうな問題でしたが、電子数を数えれば正解にたどり着けますね。
---
YouTubeでショート動画を始めました!
第109回薬剤師国家試験の解説をしていますので、是非どうぞ↓
本ブログの管理人が薬の書籍を執筆しました↓(2024年9月発売)
薬理学を簡単に説明しつつ、有機化学(医薬品化学)も織り交ぜています。
こちらも是非よろしくお願いします!
noteではサイエンスライターとして、薬をはじめとする様々な情報を発信しています↓
こちらもよろしくお願いします。
問題の出典: 厚生労働省ホームページ(https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000198920.html)
*1:参考: 第104回問6、選択肢4と5
